
ヒトは色々な病気にかかります。
糖尿病や高血圧症といった多くの方が罹患する恐れのものもあれば、10万人、100万人に1人しか罹患しないような疾患もあります。
かくいう私も10万人に1人の疾患に罹患し、過去に半日に渡る手術を受けたことがあります。
おかげさまで毎日平和に暮らしているわけですが、おまけで頭痛と片方の耳鳴りが持病になりました。
でも医薬品開発に従事する身としては、非常に有意義な経験でした。
製薬会社はボランティア企業ではありませんので、医薬品の開発には利益を求めます。
より患者が多い疾患の治療薬にリソースを割こうとするのは当然です。
しかし製薬企業は、ヒトの健康に寄与する企業としての社会的な責任があります。
儲からないからといって、希少な疾患に対する医薬品を開発しないことは許されないのです。
今日はそんな希少な疾患に対する医薬品の開発にフォーカスを当ててみましょう。
Contents
オーファン・ドラッグ(Orphan Drug)とは?
オーファン・ドラッグとは希少疾病用医薬品とも呼ばれ、難病といわれるような、患者さんの数が少なく治療法も確立されていない病気のための医薬品のことをいいます。
オーファンは日本語では「孤児」と訳されます。
あまりよい言い方ではありませんが、希少疾病用の医薬品は積極的に開発できない、
つまり「見捨てられた孤児」のような医薬品ということで、オーファン・ドラッグと呼ばれているのです。
オーファン・ドラッグの指定基準
オーファン・ドラッグのして基準は下記のとおりです。
一番分かりやすいのが「対象患者数が5万人未満」というところですね。
患者さんがとにかく少ないということです。
そして疾患としては重篤であり、医療上の必要性が高いにもかかわらず、代替する医薬品や治療方法がない。
まさに見捨てられたといっても過言ではない状態ということです。
ここに光を差し込むのが、我々製薬企業の社会的な責任の一つなのですね。
近年承認されたオーファン・ドラッグ
参考:
Q54 「オーファン・ドラッグ」とは、どのようなくすりですか。 | くすりについて | 日本製薬工業協会
さて、オーファン・ドラッグがどんなものかは何となくご理解頂けたとは思いますが、実際にどんな医薬品が該当するかイメージがつきにくいかと思いますので、製薬協のページから抜粋してきました。
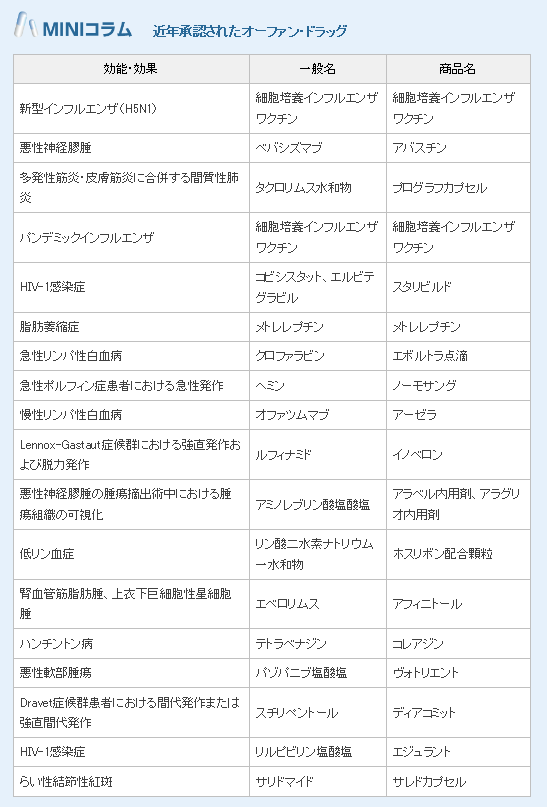
ご存知のものはありましたか?
恐らくよほどのことがないと業界外の方では知らない疾患、適応なのではないかと思います。
これが「希少疾患ということ」ですね。
適応は知らなくとも、医薬品の名前は聞いたこともあるのではないでしょうか?
ドラッグリポジショニングによる適応追加が進んでいると言えるのかもしれませんね。
参考:ドラッグリポジショニング
https://www.luna1105kablog.com/entry/drug-repositioning
以前アビガンの催奇形成の記事で、サリドマイドの適応について少し触れたような気がします。
参考:サリドマイド
https://www.luna1105kablog.com/entry/thalidomide
実はこの適応はオーファンだったのですねー!
オーファン・ドラッグの開発の課題
患者さんの数にかかわらず、病気の治療における医薬品の重要性は変わりません。
治療が困難な難病に苦しむ患者さんに手を差し伸べるという意味では、オーファン・ドラッグの開発が意義深いことは疑いの余地はないかと思います。
しかし現実はそう簡単ではありません。
多くの壁が立ちはだかっているのです。
コストの問題
新薬の開発には莫大な費用や時間が必要です。
仮に成功したとしても売れない薬に多くのリソースを割く余裕はないのです。
オーファン・ドラッグに開発リソースを費やすということは、他の薬剤の開発を遅らせることにもなり、結果的に他の薬の足を引っ張ることにもなり得ます。
難易度の問題
希少疾患に対する医薬品の開発は非常に難しいです。
そもそもその領域の知見(治験)が不足していますので、評価系から考えなければならないこともあります。
患者さんも少ないため、治験に組み入れる患者さんが足りずに、治験が難航する恐れもあります。
外野の問題
私の大嫌いな薬害オンブズパーソンのれんちゅ・・・人々は下記のように述べています。
「有効性、安全性が十分確認できないままオーファンドラッグとして開発され市場に出された新薬が適応拡大により、より多くの患者数の疾患にも使用され、莫大な利益もあげている現実も見逃してはならない」
引用している前文(アーサー・カプラン氏による論説)を読むと、製薬企業が制度を悪用しているような記載も見受けられます。
コストや難易度で開発が困難なこと以外にも、ケチをつけてくる輩もいるのですね。
ちなみに薬害オンブズパーソンはかのHPVワクチンにも当然のように難癖をつけてきています。
オーファン・ドラッグの優遇措置
日本では、1979年に難病に対する新薬研究開発事業がスタートし、1985年には承認審査の簡素化、1993年の薬事法(現在の薬機法)の改正により、オーファン・ドラッグに対する公的研究開発援助制度が始まっています。
具体的には下記のような援助制度があります。
試験計画に対する指導・助言
通常品目に優先して、随時対面助言の申し込みができます。
しかもお値打ち価格なのです!
助成金の交付
医薬基盤・健康・栄養研究所を通じて助成金の交付を受けることができます
税制措置
試験研究費総額(医薬基盤・基盤・栄養研究所の助成金を除く。)の20%を税額控除額として算定できます。
優先審査
通常は約1年かかりますが、9か月ほどで審査が完了します。
しかもお値打ち(略)
再審査期間の延長
通常品目は8年ですが、10年に延長されます。
参考:
希少疾病用医薬品・希少疾病用医療機器・希少疾病用再生医療等製品の指定制度の概要
今後はどうすればいいの?(私見)
ではオーファン・ドラッグの開発を促進するためにはどうすればよいでしょうか?
ここからは私見です。
実現が難しいものもあるでしょうし、効果が少ないのもあるかもしれません。
アカデミアと製薬企業の橋渡し
製薬企業が希少疾患の医薬品開発をゼロからスタートするのはかなり難しいように感じています。
一方でアカデミアでは病因の解明のための基礎研究やシーズとなる化合物の探索も行われています。
ただ特許の記事でも触れたように、アカデミアと製薬企業では深い谷があるように思えます。
製薬企業の持つ創薬技術とアカデミアの基礎研究、
ここの橋渡しがもっとうまくできないかな?
希少疾患の啓発
意外と軽視されがちですが、希少疾患の啓発も重要ではないでしょうか。
製薬企業や医療関係者だけではなく、患者さん自身も自分の疾患について知らないかもしれません。
それは適切な治療を受けられないだけではなく、医薬品の開発環境の悪化にもつながると思います。
これは企業がすぐにでもできることです。
自社で開発しているオーファン・ドラッグがあるのであれば、ぜひ積極的に啓発活動をしてほしいところです。
それは患者さんのためになるのは当然として、承認後の売り上げにも結び付くかもしれません。
地道な活動が重要だと思います。
インセンティブの増加
既に様々な優遇策がありますが、それでも現状、積極的に狙っていけるかというと、難しいと思います。
そもそも市場としてはかなり小さいわけですので、もう少しインセンティブがあっても良いかと思います。
ジェネリックはあまり参入しないのでその点は大丈夫でしょうか?
ジェネリックは患者さんのためと言いますが、儲からない薬にはあまり参入しないですよね。
私はそれでもいいと思います。
取りあえず、出している製品をちゃんと供給して?
まとめ
今日はオーファン・ドラッグについて取り上げてみました。
希少な疾患は自分には関係ない!と思わないでほしいなと思います。
「治療薬のない疾患の絶望感は非常に大きい」と思います。
そんな暗闇に一条の光を差し込むのが、オーファン・ドラッグなのかもしれませんね。
オーファン・ドラッグの開発には企業の体力も必要ですので、大手の製薬会社こそ力を入れて取り組んでいきたいですね!!
※当ブログにおける見解は個人的見解であり、所属する企業の見解ではございません。また特定の銘柄の購入を推奨するものではありません。








