
COVID-19蔓延下では、
- 芸能人がアビガンで回復した?からアビガンは効く!とか、
- とある専門家が効果があるといったからこの薬は有用!とか
- どこそこ病院の症例報告でシクレソニドが効いた!とか、
- 臨床試験でレムデシビルが有意差を出した!とか
色々な医学的な情報を耳にしたことがあると思います。
広義に見れば全部「エビデンス」なのかも?しれません。
しかし既にお分かりかと思いますが、このエビデンスには天と地の差があります。
今日はこのエビデンスレベルの違いについてご紹介したいと思います。
エビデンスレベルとは、簡単に言えば「研究の信頼度の目安」ですね
さまざまな団体が多様な基準を作っているので、どれが一番良いのかは分かりませんが、だいたいの方向性は同じです。
今日はエビデンスレベルの1例として、「診療ガイドライン作成の手引き2014」で採用されているエビデンスレベルをもとに、中身を見ていきましょう。
数が小さいほどエビデンスレベルは高くなります。
Contents
1.メタアナリシス
いきなり横文字が出てきて、お帰りの準備をはじめた方がおられるかもしれませんが、
今日の内容は難解ですので、
- 専門家の意見が一番レベルとして低いため、メディアの情報を鵜呑みにしないで!
- ある疾患にある薬を投与して改善が見られたからといって、その薬が効果的であったとはいえない!
ということだけ持って帰っていただければ大丈夫です。
ではメタアナリシスについて見ていきましょう。
メタアナリシスとは複数の研究を統合して統計解析を行う手法です。
システマティックレビュー、系統的総説とも言われます。
「信頼ある研究」を統合して解析を行えば、母数も増えますし、信頼性は上がっていきます。
感覚的にも分かりますよね?
雑に言えば、「みんなで力を合わせれば大きな結果が出せる」のです。
ただし、個々の研究の質や均一性に影響されます。
統合するランダム化比較試験における結果の信頼性が劣るものがあると、それに引っ張られてしまうということです。
要は「プロジェクトに参加しているやつに無能がいると台無しになる」のです。
あ、だんだん口が悪くなってきました。
ごめんなさい。
うん!みんなで一つのチームです!よね?
分かりにくいかと思いますので、事例を出しましょう。
下記は睡眠時間の短さと亡くなる率の関係を示したものです。
(Sleep duration and mortality: a systematic review and meta-analysis.J Sleep Res. 2009 Jun;18(2):148-58)
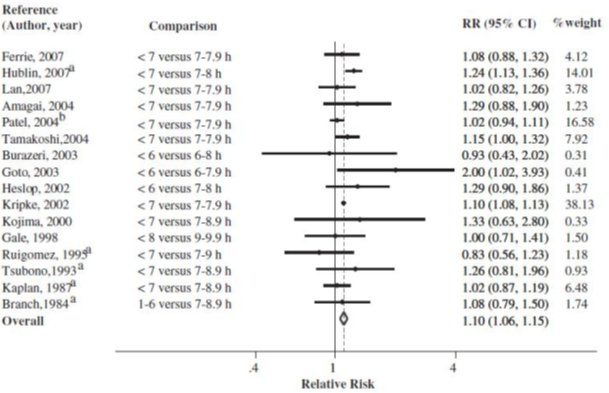
短い睡眠時間のほうがリスク比が高いという結果が出ました。
複数の研究を統合することで、このような結果が出せるのですね。
メタアナリシスが有用なケースとしては、下記のようなものが挙げられます。
- 複数の研究で得られた効果が一致しない場合
- 個々の研究の標本サイズが小さく有意な効果を見いだせない場合
- 大きな標本サイズの研究が経済的・時間的に困難な場合
ただしメタアナリシスにはバイアスが入ります。
何でだと思いますか?
これは報告される研究は、ほとんどが良い結果だからです!
このバイアスは時に軽視されがちなので、注意しなければなりません。
研究者がポジティブな結果が得られたときにのみ発表する「報告バイアス」
学会誌等の編集者が、統計学的に有意な結果の得られていないものはrejectする「出版バイアス」
こんなバイアスには注意が必要ですね。
現在はバイアスが減らせるように試験をデータベースに登録するようになっているそうです。
2.ランダム化比較試験
これはランダム化(無作為化)された臨床試験のことです。
ある薬剤と対照薬の2つがあって、患者さんをどちらの群に割り当てるかというところに、作為的な意図を含めない手法です。
これをすることで、割り付けによるバイアスを低減することができます。
簡単に言えば、この人は効きそうだから治験薬群にして、この人は微妙だから対照群にしよう!といいうことができなくなります。
いわゆる一般的な臨床試験ですね!
3.非ランダム化比較試験
こちらは読んで字のごとく、割り付けが非ランダム化、つまり人為的に決めている試験です。
当然バイアスの影響は無視できません。
大して変わらないと思ってはいけません。
人は機械ではないので、バイアスの力はとても大きいのです。
4.分析疫学的研究
さて、ここからは更に難解になります。
でもここまでお付き合いいただいたからには最後までお付き合いください。
あと変なところがあったら指摘してください。
私も若干背伸びしています。
さて、分析疫学について、日本疫学会の説明を借りますと、
「分析疫学とは記述疫学などから得られた、関連があると疑われた要因(仮説要因)と疾病との統計学的関連を確かめ、要因の因果性を推定する方法であり、仮説の検証を主な目的」とするものです。
「記述疫学で明確にした4つのW(When, Where, Who, What)をもとに、Whyを追究する」のです
記述疫学では仮説を得て、それを検証するのが分析疫学ということですね。
これではイメージがつきにくいので、具体的な研究手法について事例を挙げつつ見てみましょう。
前向きコホート研究
将来に向かって問題とする疾病の発生を観察する方法です。
コホート(cohort)とは同一条件に規定された群(集団)のことです。
起点を研究開始時点として、将来渡って暴露の影響を見ていくのです。
例えば、特定の癌の発生に喫煙が関係すると考えられる場合、現在癌の患者ではない人を募集し、喫煙習慣のある人とない人で、癌の罹患率に差があるかどうかを将来にわたって追跡・検討する研究とかですね。
余談ですが、イソジン騒動の時に介入研究か観察研究かで議論がありましたね。
コホート研究は観察研究です。
対象集団に手を加えることなく、「観察」するからです。
イソジンの研究は、私は介入研究ではないかと思います。
イソジンによるうがいを介入ではないと言えるのかしら?
症例対照研究
症例対照研究とは、疾病の原因を過去にさかのぼって探そうとする研究のことです。
コホート研究は未来を見ていたので、その逆ということですね!
しかし後ろ向きコホートと同義ではありません。
後ろ向きコホートは現在から過去のコホートを探し、現在の疾患の発生状況を探します。
例えば、後ろ向きコホートの例としては、過去にダイオキシンに高濃度に曝露された集団を対象に追跡調査を行い、疾病の罹患を確認したりする研究とかですね。
後ろ向きの研究は過去の時点からのお話ですので、交絡因子のコントロールなどが難しいので、エビデンスとしては少し落ちますね。
症例対照研究は、目的とする疾病(健康障害)の患者集団とその疾病に罹患したことのない人の集団を選び、仮説が設定された要因に曝露されたものの割合を両群比較します。
例えば、過去と現在の肥満と心筋梗塞のリスクの関係を明らかにすることを目的として、
急性心筋梗塞患者で、過去に心筋梗塞の既往のない人から生活暦(飲酒、喫煙など)、既往歴(高血圧、糖尿病、高脂血症など)、身長、体重、10年前の体重などの情報を収集し、
同時に性、年齢、居住区域をマッチさせた対照群からも同様の情報を得てリスクの比較をする研究などが挙げられますね。
ややこしいですね。
- 過去に起点を置き、そこから暴露、非暴露の群の経過を追っていくのが後ろ向きコホート、
- 現在の疾病のありなしから、過去の要因の暴露状況について確認するのが疾病対象研究
こんな感じですね!(あってます?)
5.記述研究(症例報告やケース・シリーズ)
これがよくニュースで流れるものです。
例えば、ある症例(複数であることも)に対して、ある薬剤を投与したら効きました!という情報です。
これはその薬が効いたのか、他の治療が効いたのかまるで分かりません。
比較対象がいないからです。
もしかしたら自然治癒かもしれません。
特にCOVID-19は8割が軽症で自然治癒すると考えられています。
非常に大事なことですが、「ある疾患にある薬を投与して改善が見られたからといって、その薬が効果的であったとはいえない」のです!
これを勘違いしている人はいまだ無数にいます。
昨今の低レベルなメディアにおいても良く見られますね。
むしろ誤解を招く諸悪の根源でしょう。
6. 患者データに基づかない、専門委員会や専門家個人の意見
専門家の個人的見解がこちらになります。
もっともレベルの低い、エビデンスというのもおこがましいレベルです。
「アビガンが効くから早く承認しろ」という、某ノーベル賞受賞者の意見等がこちらに分類されます。
いや、この分野において専門家ではないわけですので、ここに分類してはならないのかもしれません。
分野の権威の意見とかになりますかね?
134:素人の戯言
とある芸能人のアビガン服薬で治りました!等というものは、エビデンスにすらなり得ないただの戯言です。
これをもとにアビガンを早く承認しろー!とか、承認されないのは製薬会社の利権だなんだと騒がれるのは、
何て返せばよいのでしょうか。
少なくとも科学的な側面から見れば、報道する価値は欠片もないと思います。
芸能ニュースならどうぞご自由にとも思いますが、勘違いされる方もいるので、きちんと科学的に補足頂きたかったですね
(そんなことがメディアにできたとは思えませんが)
おまけ:ネットワークメタアナリシス
メタアナリシスは事象間の直接比較を行いますが、間接比較を用いることで複数の事象を評価することができる手法として、ネットワークメタアナリシスという手法もあります。
間接比較を用いるということは、全ての事象間でInconsistency(矛盾)がないという仮定が必要ですので、ネットワークメタアナリシスにおける順位付けを絶対の指標に用いてはならないと思います。
この件は下記の記事でも触れています。

まとめ
今日はエビデンスのレベルについて見てきました。
・・・専門家、論文、研究。
ぱっと聞くとどれも権威ある人による「確固たるエビデンス」が作られているように聞こえますよね?
でもそんなことはないのです。
「専門家」を素人と比べるから、権威がある信用が厚いものと誤解してしまうのです。
「論文」をその辺の雑誌と比べるからいけないのです。
「研究」の比較すべきは自由研究ではありません。
エビデンスレベルとは、専門家、論文、研究の「中でのレベル」です。
その外と比べても仕方ありません。
権威に騙されるのはそれ以前の問題ということです。
診療ガイドラインで推奨されるような治療法は、だいたいにおいて、少なくとも1つの質の高い無作為比較試験が報告されていると思います。
そうでない場合は必ず注意書きがあります。
逆に言えば、無作為化臨床試験が行われていないような治療法はエビデンスレベルが低く、推奨度合いとしては低いということです。
〇〇が効果がある!
〇〇がCOVID-19の治療薬候補として挙がった!
そんな報道を見た時、よく考えてみてください。
私見ではありますが、今のメディアにエビデンスレベルを正しく報道できる力はあるとは到底思えません。
少なくとも日本のメディアには。
私たち、受け手側がきちんと情報を吟味する必要があるのです。
何だか重い内容になってしまった気がしますが、私ではこれ以上噛み砕いて説明するのは難しいです。
取りあえず、途中でも挙げた下記の2点をご理解頂ければ、私としては満足です!
- 専門家の意見が一番レベルとして低いので、それを報道するメディアの情報を鵜呑みにしないで!
- ある疾患にある薬を投与して改善が見られたからといって、その薬が効果的であったとはいえない!
そのうちメディアも理解してもらえると嬉しいな。
そんな日は果たして来るのでしょうか?
※当ブログにおける見解は個人的見解であり、所属する企業の見解ではございません。また特定の銘柄の購入を推奨するものではありません。








